- Inici
- Genètica: present i futur
- Clonatge i cèl·lules mare
Clonatge i cèl·lules mare
Què és el clonatge?
El clonatge és un conjunt de tècniques de laboratori que ens permet reproduir tantes vegades com vulguem un material biològic en concret: cèl·lules, ADN, etc.
Podríem dir que l’acte de clonar equival al de fotocopiar, és a dir, treure moltes còpies idèntiques d’alguna cosa que ens interessa.
I en el nostre cas, què és el que volem clonar o fotocopiar?
Doncs és molt fàcil! Unes cèl·lules anomenades cèl·lules mare.
Què són les cèl·lules mare?
Són cèl·lules bastant indiferenciades o no especialitzades, és a dir sense funció pròpia, perquè encara no s’han convertit en cèl·lules d’un teixit específic.
Es diferencien de la resta de les altres cèl·lules corporals perquè al dividir-se presenten les següents propietats:
- Produir noves còpies d’elles mateixes de forma indefinida.
- Produir noves cèl·lules que, mitjançant els estímuls apropiats, es transformaran en els diferents teixits de què està compost el cos humà.
- Poden colonitzar i reparar un teixit o un òrgan malalt substituint les cèl.lules malaltes per cèl.lules sanes.
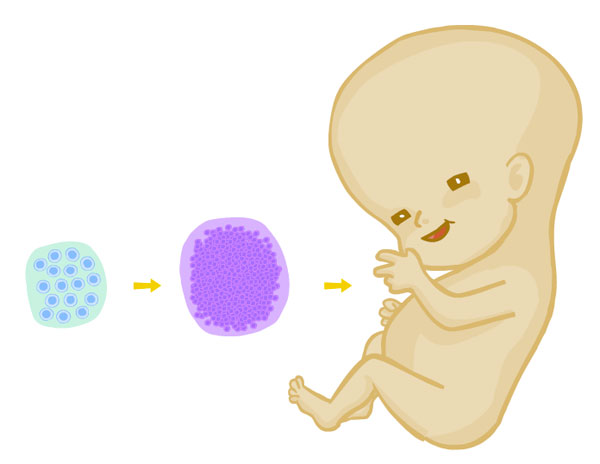
Les cèl·lules mare són les cèl·lules a partir de les quals ens hem desenvolupat cadascun de nosaltres quan es van unir l’òvul i l’espermatozoide, i són les cèl·lules que van donar lloc a tots els òrgans i teixits del nostre cos quan van ser sotmeses als estímuls específics necessaris per a això. Tots els nostres òrgans i teixits en conserven una “petita reserva” que els permeten mantenir-les i reparar-les.
Per què estem tan interessats en el clonatge de les cèl·lules mare?
Perquè les cèl·lules mare, juntament amb la manipulació genètica, seran dos pilars fonamentals de la medicina en els propers anys.
Perquè quan combinem de manera apropiada tots els coneixements de què disposem sobre genètica, medicina, física, química, biologia molecular, enginyeria cel·lular i tissular, bioquímica, etc., a partir d’una o molt poques cèl·lules, podrem dissenyar i produir tantes cèl·lules com necessitem per reparar els teixits, òrgans o estructures danyats del nostre cos; això s’anomena medicina regenerativa o reparativa.

Per exemple, en la malaltia de Parkinson, les cèl·lules nervioses que fallen podran ser substituïdes per cèl·lules nervioses noves, i l’individu en qüestió es curarà.
Les cèl.lules cardíaques danyades per infarts o per insuficiència cardíaca podran ser substituïdes per cèl.lules cardíaques noves i l’individu en qüestió es guarirà.
Podrem reparar les lesions medul.lars produïdes per tumors i accidents. A les persones diabètiques els podrem transplantar cèl.lules productores d’insulina en el seu pàncrees i l’individu en qüestió es guarirà.
I el mateix passarà amb moltes altres patològies: càncer, fibrosi quística, malalties degeneratives com per exemple l’Alzheimer, etc.
En quin punt ens trobem?
Sabem que les cèl·lules del nostre cos, durant la seva especialització o transformació, estan sotmeses a una programació cel·lular organoespecífica,
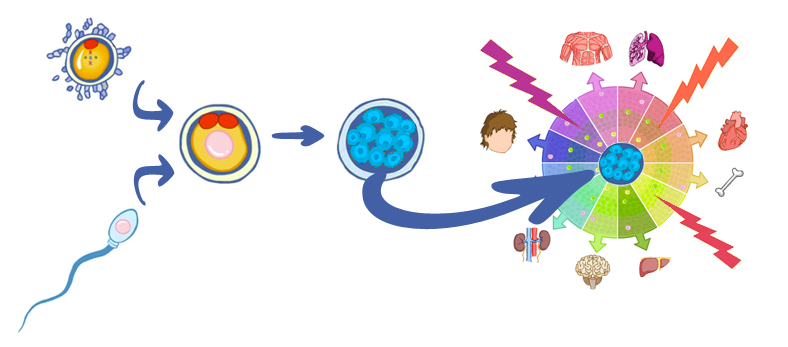
I que totes les cèl·lules del nostre cos s’han desenvolupat a partir d’una única cèl·lula “l’ou o òvul fertilitzat per un espermatozoide”, per la qual cosa totes són idèntiques, és a dir, posseeixen exactament les mateixes instruccions, però, depenent de l’òrgan del qual formin part, utilitzaran només una part de la informació o una altra. Això es coneix com a especialització cel·lular.
És a dir, tota cèl·lula humana té 46 cromosomes gravats amb totes les nostres receptes de cuina (gens). Tanmateix, aquestes receptes no s’expressen alhora en totes les cèl·lules, sinó que en unes cèl·lules s’expressen i funcionen unes, i en altres cèl·lules s’expressen i funcionen d’altres.
Així, un pulmó és diferent d’un ull, perquè al pulmó les receptes són per a la formació de cèl·lules especialitzades en la respiració, en canvi en l’ull les receptes que es posen en marxa són per formar un òrgan que ens permeti la visió.
És a dir, a partir d’una cèl.lula indiferenciada, es desenvolupa un individu complet amb milions de cèl.lules diferenciades que formen part de diferents estructures. Això significa que durant aquest procés les cèl.lules s’han anat especialitzant.
Per tant, des del moment de la fecundació fins al naixement d’un individu i durant tota la vida d’aquest, les cèl·lules estan sotmeses a un procés continu de diferenciació o especialització cel·lular sota les ordres d’una programació cel·lular concreta per a cada espècie.
Aquestes cèl·lules, en les seves primeres fases de desenvolupament embrionari, es caracteritzen per tenir tot el seu potencial i ser verges, és a dir, tenen la capacitat de produir un ésser viu complet i són capaces de donar origen a tots els teixits o estructures del nou individu, incloses les membranes extraembrionàries que formen la placenta, per això se les anomena cèl·lules mare totipotencials. Després, a mesura que la gestació avança, van perdent part d’aquest potencial perquè cada vegada estan més especialitzades, i partint de les seves possibilitats de transformació o diferenciació van rebent diferents noms:
- Entenem per cèl·lules mare pluripotencials aquelles amb capacitat per transformar-se en tots els teixits que componen un ésser viu, excepte els teixits extraembrionaris (placenta).
- Entenem per cèl·lules mare multipotencials aquelles que poden diferenciar-se o transformar-se en alguns teixits, però ja no en tots.
- I, per cèl·lules mare unipotencials, aquelles que poden transformar-se en un sol tipus de teixit cel·lular.
I això què significa?
Doncs ni més ni menys!:
- QUE si aprenem com estimular, programar i desprogramar aquestes cèl·lules mare, en un futur podrem generar ,a nivell mundial, teixits terapèutics, òrgans de recanvi, noves cèl.lules que colonitzaran i repararan els teixits danyats o malalts i nous medicaments i proteïnes terapèutiques.
- QUE si aconseguim desenvolupar nous mètodes d’enginyeria genètica amb fins de teràpia gènica, podrem corregir les errades genètiques de les cèl.lules mare abans de la seva diferenciació en teixits o òrgans específics, amb la qual cosa evitarem malalties o malformacions.
- QUE si, a més, això ho aconseguim amb les cèl·lules mare que té cada ésser humà en alguns dels seus teixits, li podrem reparar tots els teixits o òrgans danyats amb les seves pròpies cèl·lules , amb la qual cosa el problema actual del rebuig immunològic amb les cèl·lules de donant, i les llargues llistes d’espera per al trasplantament d’òrgans al igual que la venda il.legal d’òrgans al mercat negre s’haurà acabat.
Us imagineu el dia en què aconseguim desprogramar sense efectes secundaris o col·laterals una cèl·lula ja programada per tornar a programar-la segons les nostres conveniències?
Totes les cèl.lules mare són iguals o n’hi ha de diferents tipus?
N’hi ha de tres tipus segons el moment en què es puguin obtenir:
- Les cèl·lules mare embrionàries.
- Les cèl·lules mare adultes o somàtiques.
- oLes cèl·lules mare pluripotents induïdes, també conegudes com a cèl·lules iPS.
En què es distingeixen?
- Bàsicament en la capacitat potencial (totipotencial, pluripotencial, multipotencial, unipotencial) que posseeix cada una d’ elles per transformar-se en els diferents tipus de cèl.lules o teixits que formen el nostre cos.
- La seva diferent capacitat per autorenovar-se (produir noves còpies d’elles mateixes).
Les cèl·lules mare embrionàries i les cèl·lules mare adultes o somàtiques són d’origen natural. Les cèl·lules mare pluripotents induïdes són d’origen artificial o induïdes en el laboratori.
Vegem-ho:
Les cèl·lules mare embrionàries i les cèl·lules mare adultes o somàtiques són naturals, pel que fa al seu origen, és a dir són les mateixes cèl·lules mare que reben diferents noms segons l’estadi evolutiu maduratiu en què es troben: embrió – fetus – nen – adult – cadàver, sense ser manipulades per l’home, és a dir simplement seguint el seu procés natural.
Quan aquestes formen part de l’embrió s’anomenen cèl·lules mare embrionàries.
Quan aquestes formen part dels teixits dels fetus, nens, adults, cordons umbilicals, placentes i cadàvers s’anomenen cèl·lules mare adultes o somàtiques. Cada teixit o òrgan del nostre cos adult (postnatal) té una reserva cel·lular d’aquestes cèl·lules, i amb aquestes substituïm les nostres cèl·lules malaltes o mortes i reparem òrgans lesionats de manera natural; per exemple, quan ens trenquem un os aquest torna a soldar-se, quan ens lesionem la pell o el múscul, aquest cicatritza i pell i múscul tornen a regenerar-se, etc.
Les cèl·lules mare pluripotents induïdes són cèl·lules manipulades (artificials), ja que s’han aconseguit en el laboratori desprogramant cèl·lules mare adultes.
I mentrestant, què?
Doncs, cal investigar i aprendre a reconèixer quins són tots els senyals a què se sotmet una cèl·lula per formar un òrgan específic.
D’on podem obtenir CÈL·LULES MARE per investigar i aconseguir el nostre objectiu?
Doncs, és molt fàcil! A partir de:
- Embrions
- Fetus
- Líquid amniòtic
- Sang del cordó umbilical
- Teixit del cordó umbilical
- Teixit placentari
- Individus adults
- Cèl·lules iPS (Cèl·lules adultes reprogramades)
Els embrions són la font de les CÈL.LULES MARE EMBRIONÀRIES.
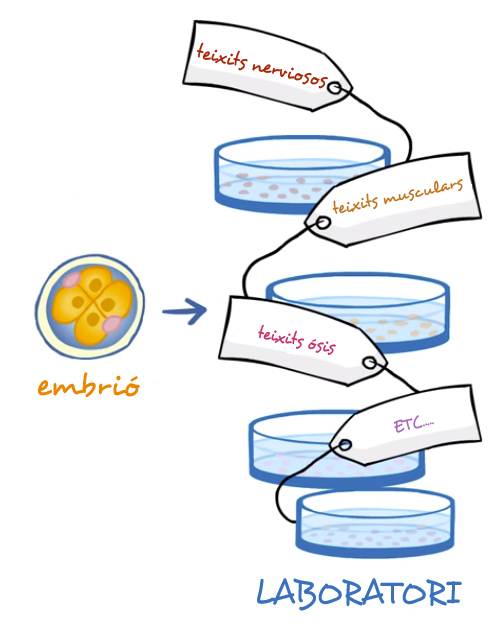
Per obtenir cèl.lules embrionàries, primer necessitem fabricar embrions i després deixar-los créixer durant 5-7 dies al laboratori perquè es desenvolupin i es transformin en un blastocist.
Quan s’ha aconseguit es destrueix l’embrió i s’agafen unes cèl.lules que es troben a l’interior conegudes com massa cel.lular interna, per tal de cultivar-les al laboratori. Aquestes cèl.lules són l’origen de les cèl.lules mare embrionàries.
I, com podem fabricar els embrions?
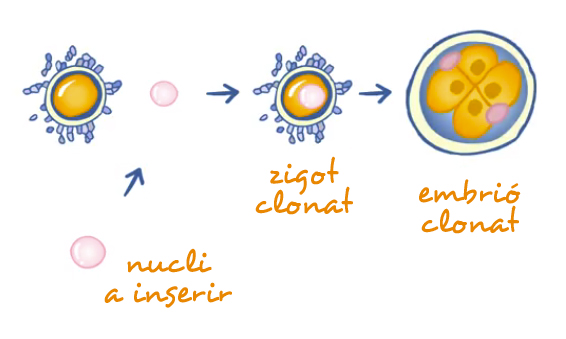
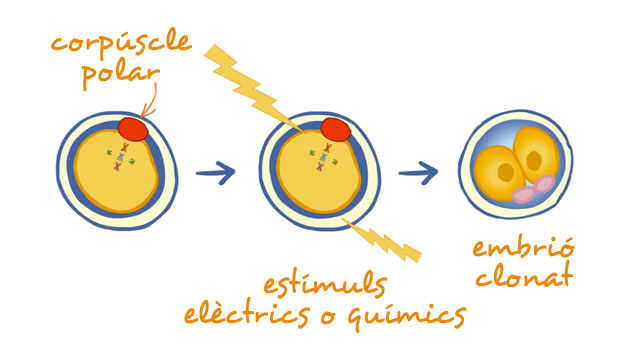
Molt fàcil, ho podem fer al laboratori utilitzant alguna d’aquestes tècniques:
Quan s’hagi obtingut l’embrió, segons el seu destí final, es podran fer dos tipus de clonació:
La utilització d’aquesta tecnologia presenta dilemes ètics i morals.
Per obtenir més informació, consulteu els enllaços reacionats en l’apartat.
Els teixits o òrgans fetals s’obtenen a partir de fetus que han estat avortats i poden proporcionar DOS tipus de cèl.lules mare: les cèl.lules mare embrionàries germinals (amb característiques de cèl.lules mare embrionàries) i les cèl.lules mare adultes o somàtiques.
- Les CÈL.LULES MARE EMBRIONÀRIES GERMINALS son les que s’obtenen en embrions – fetus amb una edat d’entre 5 i 10 setmanes de gestació, a partir d’una estructura anatòmica anomenada cresta gonadal. Aquestes cèl.lules, en condicions normals, són les que, durant la vida fèrtil de l’individu, donen òvuls i espermatozoides.
- Les CÈL.LULES MARE ADULTES o SOMÀTIQUES són les que s’obtenen a partir de les restes dels teixits fetals en fetus de qualsevol edat. Les cèl.lules mare adultes provinents de teixits fetals tenen menys potencialitat que les cèl.lules mare embrionàries perquè estan més diferenciades. Convé dir que estan donant bons resultats.
Alguns experiments informen que el transplantament de cèl.lules neuronals provinents de fetus humans tenen un efecte terapèutic en pacients amb Parkinson, amb una important reducció dels símptomes de la malaltia en pacients tractats.
Malgrat tot, la consecució de teixit neuronal fetal i teixits fetals en general és molt limitada. Alguns grups antiavortistes s’oposen totalment a l’obtenció d’aquest tipus de cèl.lules per tal d’evitar que moltes dones siguin induïdes a l’avortament de fetus sans amb la finalitat d’obtenir i vendre aquest tipus de teixits en mercats negres il.legals.
Recentment, s’ha tingut constància que en el líquid amniòtic hi ha cèl·lules mare fetals mesenquimàtiques, semblants a les cèl·lules mare embrionàries, és a dir, cèl·lules pluripotencials que, sota els estímuls apropiats, podrien convertir-se en les futures cèl·lules reparadores dels diversos teixits del cos humà.
En aquest moment, el potencial en aquesta àrea d’investigació és immens:
- Doncs aquestes cèl·lules són molt semblants a les cèl·lules mare embrionàries respecte al seu potencial de creixement i diferenciació, amb l’avantatge afegit que, en desenvolpar-se no creen tumors.
- En cas de necessitat, si durant la gestació es detectés algun nen malalt, aquestes cèl·lules podrien ser extretes del líquid amniòtic, reprogramar-les i ser usades durant la mateixa gestació per evitar l’avanç de la patologia, i, si això no fos possible, tenir-les preparades per quan neixi el bebè.
- A més, aquestes cèl·lules no presentarien cap risc immonològic per al nen originat per aquesta gestació, ja que són cèl·lules procedents de la seva pròpia placenta i del seu propi líquid amniòtic.
- Aquestes cèl·lules podrien ser guardades en bancs cel·lulars, igual que les cèl·lules mare procedents del cordó umbilical, que constituirien una reserva de teixits immunològicament compatibles per a la població mundial.
- Tampoc hi hauria cap problema des del punt de vista ètic, ja que el seu ús no suposa la destrucció de l’embrió i hi ha estudis que assenyalen que aquestes cèl·lules també poden obtenir-se de la placenta després del part, a més del líquid amniòtic.
Els primers experiments amb aquestes cèl·lules ja s’han dut a terme amb ratolins.
La sang del cordó umbilical és una font de CÈL.LULES MARE ADULTES o SOMÀTIQUES.
L’obtenció d’aquestes cèl.lules no planteja cap dilema ètic i legal, i estan oferint bons resultats.
S’obtenen mitjançant la punció de la vena del cordó umbilical durant els quinze minuts posteriors al naixement del nen.
Com que aquestes cèl.lules posseeixen un gran potencial terapèutic per a la població mundial i per al donant i la seva família, us recomanem que entreu en els enllaços següents i valoreu la seva informació.
Les cèl·lules de teixits de cordó umbilical són una font de CÈL·LULES MARE ADULTES o SOMÀTIQUES.
Aquest teixit està compost per diferents tipus de cèl·lules que poden tenir diferents usos potencials, tots ells actualment en fase d’investigació.
Les cèl·lules procedents de teixit placentari són una font de CÈL·LULES MARE ADULTES o SOMÀTIQUES.
Totes aquests cèl·lules estan en fase d’investigació.
Els teixits i òrgans dels individus adults proporcionen CÈL.LULES MARE ADULTES o SOMÀTIQUES.
Sabem que aquestes cèl.lules mare indifernciades formen part de teixits i organs totalment diferenciats i que a més a més:
- Els trobem en molts texits adults (medul.la òssia, sang, còrnea i retina, cervell, múscul esquelètic, pulpa dental, fetge, epiteli de la pell, i del sistema digestiu, pàncrees i teixit adipós) i se’n van descobrint de nous.
- Són les encarregades de mantenir la viabilitat dels teixits sotmesos a un esforç i renovació constant, com la pell, la sang (medul.la òssia), la mucosa intestinal, el cervell, el teixit adipós, etc.
- Estan implicades en la regeneració del teixit danyat.
- Tenen moltes més propietats de les que en un principi es va pensar, com la plasticitat, capacitat de produir teixits de diferent llinatge, quan se les aïlla del teixit de què formen part i se les sotmet als estímuls oportuns.
La seva obtenció no planteja cap dilema ètic ni moral i es poden obtenir a partir del teixit apropiat, tant d’individus vius com morts, els primers mitjançant la donació, els segons mitjançant l’autòpsia.
Si voleu més informació us recomanem que visiteu els enllaços relacionats.
Què són les cèl·lules mare pluripotents induïdes?
Les cèl·lules mare pluripotents induïdes (iPSC) són cèl·lules que han estat sotmeses a una reprogramació genètica per fer-les retrocedir en el temps i tornar-les a un estat similar al que tenien quan eren cèl·lules mare embrionàries I obligar-les així a expressar els mateixos gens i els mateixos factors que expressaven aleshores.
Què significa que han estat reprogramades o desdiferenciades a un estat similar al que tenien quan eren cèl·lules mare embrionàries?
Doncs molt fàcil, reprogramem i actualitzem els nostres coneixements:
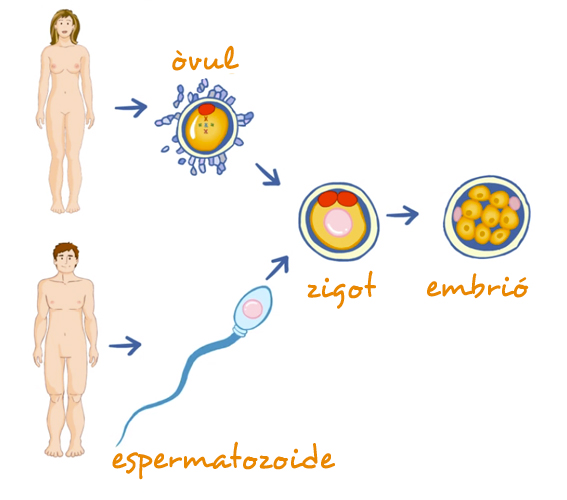
1) Sabem que en el moment de la fertitlització, quan s’uneixen l’òvul i l’espermatozoide, es forma un ou i aquest comença a dividir-se fins que es forma un individu complet.
VEGEM-HO:
2) Sabem que les cèl·lules de les primeres divisions cel·lulars que es produeixen a l’embrió tenen el potencial de poder-se convertir en qualsevol teixit del cos. I a poc a poc, a mesura que s’especialitzen en un teixit concret, van perdent aquesta propietat.
És a dir, estareu d’acord amb mi que LA CÈL·LULA S’HA ESPECIALITZAT O PROGRAMAT, oi? 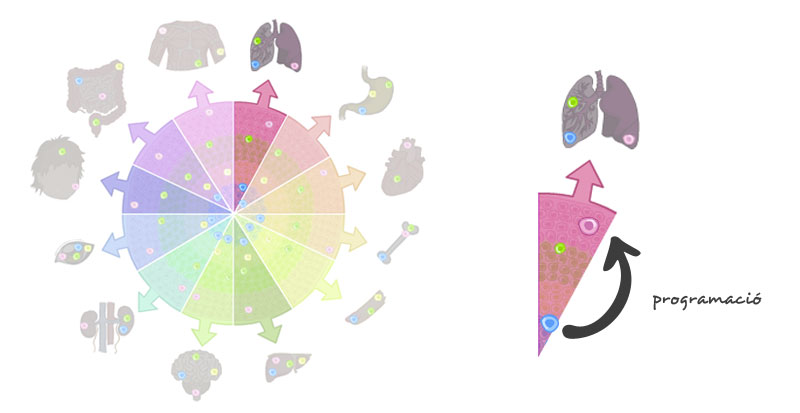 Doncs bé, ara fem el circuit al revés:
Doncs bé, ara fem el circuit al revés:
Desprogramarem una cèl·lula ADULTA ja especialitzada en un teixit concret, i la farem retrocedir en el temps fins a l’estadi de CÈL·LULA MARE EMBRIONÀRIA, fase en què tenia el potencial de convertir-se en qualsevol teixit del cos humà. Ho heu pescat? 
Doncs ni més ni menys, aquí ho teniu, aquesta cèl·lula que hem desprogramat a voluntat és la que anomenem cèl·lula mare pluripotent induïda (iPSC).
I per què estem tan interessats en l’obtenció d’aquestes cèl·lules?
Doncs perquè podrem fer medicina reparativa o regenerativa a la carta, és a dir, individualitzada.
Imagineu-vos un individu que ha patit un infart. Doncs a partir de qualsevol de les seves cèl·lules adultes (pell, múscul, etc.), per mitjà de les tècniques apropiades, podrem fer-les retrocedir en el temps i aconseguir de posar-les en la situació en què eren capaces de produir cèl·lules cardíaques. Una vegada aconseguit aquest objectiu podrem obtenir tantes cèl·lules de recanvi com calgui per poder reparar-li el cor.
I això ho podrem fer amb tots els òrgans i teixits que conformen el nostre cos.
És a dir, a partir de les cèl·lules adultes d’un individu, mitjançant la seva desprogramació i nova programació, podrem obtenir cèl·lules capaces de convertir-se en els teixits específics que ens interessin o que necessitem per ajudar-lo a sanar de la seva patologia…
I quins avantatges tenen aquestes cèl·lules sobre les altres cèl·lules mare existents
Doncs que en ser del mateix individu no hi haurà rebuig immunològic. I molt important: l’origen d’aquestes cèl·lules no planteja cap debat ètic, ja que per obtenir cèl·lules mare embrionàries s’han de destruir els embrions.
Quina aplicabilitat clínica tenen aquestes cèl·lules en aquest moment?
Cap, perquè encara estan en fase d’investigació. Abans de passar a fer-les servir en pacients, hem d’estar molt segurs que reuneixin tots els criteris de seguretat necessaris, com ara no produir càncer o certes malalties provocades pels mateixos canvis o mutacions que puguin haver-se originat durant aquest procés.
A qui més pot beneficiar treballar o investigar amb aquest tipus de cèl·lules?
Els laboratoris, ja que així poden i podran provar l’eficàcia dels medicaments sobre les cèl·lules vives dels cultius cel·lulars.
Els investigadors cel·lulars i moleculars, ja que totes aquestes estratègies els obren noves portes per aprendre com programar, desprogramar i reprogramar les cèl·lules per poder reparar els teixits danyats de l’organisme o introduir-hi noves característiques que ens interessin expressar.
Des de quan existeixen aquestes cèl·lules?
El 2006 es van registrar per primera vegada les iPSC induïdes en ratolins.
El 2007 es van registrar per primera vegada les iPSC induïdes en humans.
Si d’entre totes les cèl.lules mare disponibles en l’actualitat ens plantegem quines són les millors per als nostres propòsits, direm que en aquest moment la resposta NO existeix.
- Estem en un moment en què hi ha més preguntes que respostes. No oblidem que la biologia del desenvolupament i la enginyeria tissular són ciències de les quals encara ens queda molt per aprendre.
- Ningú sap del cert quin serà el potencial real de totes aquestes cèl.lules quan estiguin sotmeses als estímuls apropiats.
- La defensa de qualsevol tipus cel.lular específic està ple d’interessos privats per part d’aquells que els defensen, independentment del mitjà o sistema que utilitzin.
- Aquestes cèl.lules poden ser molt útils en moltes línies d’investigació, i unes poden funcionar millor que d’altres.
Per aquest motiu, el més prudent en aquests moments és escoltar, valorar i respectar totes les opinions, a més d’investigar en tots els camps per tal d’anar cap a la recerca de la veritat.
I quan sapiguem on som, decidir quin camí hem de seguir sense oblidar que l’aplicació de totes les tècniques científiques disponibles sempre ha de ser correcta des del punt de vista ètic, i fer que això es compleixi és responsabilitat de TOTS.
Igual com ja s’està fent amb les cèl·lules mare procedents del cordó umbilical, totes aquestes cèl·lules podran ser guardades en bancs cel·lulars creats amb aquesta finalitat i constituiran una gran reserva a escala mundial de teixits immunològicament compatibles per a la població general.
En aquests moments la utilització d’embrions és motiu d’enfrontament i debat entre diverses comunitats religioses, científiques i politiques, doncs des del punt de vista moral “la utilització d’un embrió suposa la seva destrucció”, i l’ús dels teixits fetals, fa temer que moltes dones siguin induïdes a l’avortament de fetus sans amb la intenció d’obtindre aquest tipus de material.
El que sí que ha de quedar clar és que durant aquest període d’aprenentatge i la seva posterior aplicació hem de ser molt cauts davant de l’enorme potencial d’aquestes tecnologies, ja que la trilogia “assaig-error, assaig-encert, mesures correctives” pot arribar a tenir conseqüències impredictibles per a la humanitat, afectant-nos a tots de moltes maneres.
Resumint …….
Preguntes relacionades
Tot seguit us recomanem que visiteu aquesta sèrie d’enllaços, ja que us poden ajudar a comprendre la magnitut del problema que us estem plantejant.
Següent tema: Genètica i càncer
Revisió: 13 de setembre de 2017